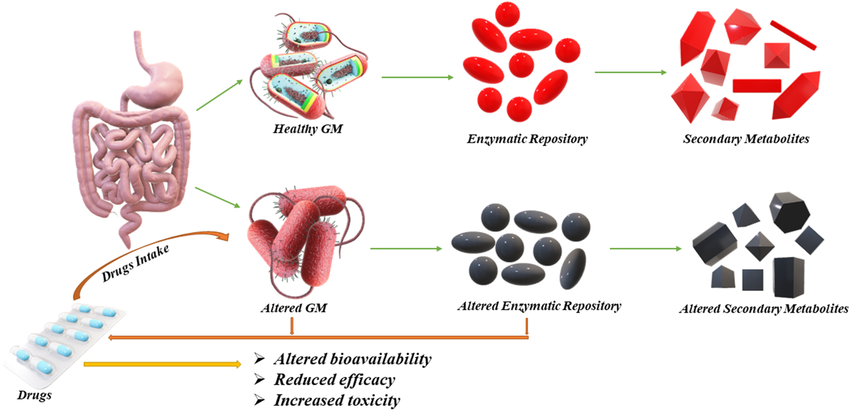
Banyak obat-obatan manusia yang dapat secara langsung menghambat pertumbuhan dan mengubah fungsi bakteri yang membentuk mikrobioma usus kita .
Para peneliti EMBL Heidelberg kini telah menemukan bahwa efek ini berkurang ketika bakteri membentuk komunitas.
Dalam studi pertama semacam ini, para peneliti dari kelompok Typas, Bork, Zimmermann, dan Savitski di EMBL Heidelberg, dan banyak alumni EMBL, termasuk Kiran Patil (Unit Toksikologi MRC Cambridge, Inggris), Sarela Garcia-Santamarina (ITQB, Portugal), André Mateus (Universitas Umeå, Swedia), serta Lisa Maier dan Ana Rita Brochado (Universitas Tübingen, Jerman), membandingkan sejumlah besar interaksi obat-mikrobioma antara bakteri yang tumbuh dalam isolasi dan bakteri yang merupakan bagian dari komunitas mikroba yang kompleks. Temuan mereka baru-baru ini dipublikasikan dalam jurnal Cell .
Dalam penelitian mereka, tim tersebut menyelidiki bagaimana 30 obat yang berbeda (termasuk yang menargetkan penyakit menular atau tidak menular) memengaruhi 32 spesies bakteri yang berbeda. Ke-32 spesies ini dipilih sebagai perwakilan mikrobioma usus manusia berdasarkan data yang tersedia di lima benua.
Mereka menemukan bahwa ketika bersama-sama, bakteri tertentu yang resistan terhadap obat menunjukkan perilaku komunal yang melindungi bakteri lain yang sensitif terhadap obat. Perilaku ‘perlindungan silang’ ini memungkinkan bakteri sensitif tersebut tumbuh secara normal ketika berada dalam komunitas dengan adanya obat yang akan membunuh mereka jika mereka diisolasi.
“Kami tidak menyangka ketahanannya begitu tinggi,” kata Sarela Garcia-Santamarina, mantan postdoc di kelompok Typas dan salah satu penulis pertama studi tersebut, yang saat ini menjadi pemimpin kelompok di Instituto de Tecnologia Química e Biológica (ITQB), Universidade Nova de Lisboa, Portugal. “Sangat mengejutkan melihat bahwa hingga setengah dari kasus di mana spesies bakteri terpengaruh oleh obat saat tumbuh sendiri, bakteri tersebut tetap tidak terpengaruh di masyarakat.”
Para peneliti kemudian menggali lebih dalam mekanisme molekuler yang mendasari perlindungan silang ini. “Bakteri saling membantu dengan menyerap atau memecah obat,” jelas Michael Kuhn, Ilmuwan Staf Riset di Bork Group dan salah satu penulis pertama studi tersebut. “Strategi ini masing-masing disebut bioakumulasi dan biotransformasi”.
Namun, kekuatan komunitas ini juga ada batasnya. Para peneliti melihat bahwa konsentrasi obat yang tinggi menyebabkan komunitas mikrobioma runtuh dan strategi perlindungan silang digantikan oleh ‘sensitisasi silang’. Dalam sensitisasi silang, bakteri yang biasanya resistan terhadap obat tertentu menjadi sensitif terhadap obat tersebut saat berada dalam suatu komunitas – kebalikan dari apa yang penulis lihat terjadi pada konsentrasi obat yang lebih rendah.
“Ini berarti bahwa komposisi komunitas tetap kuat pada konsentrasi obat yang rendah, karena masing-masing anggota komunitas dapat melindungi spesies yang sensitif,” kata Nassos Typas, seorang pemimpin kelompok EMBL dan penulis senior studi tersebut. “Namun, ketika konsentrasi obat meningkat, situasinya berbalik. Tidak hanya lebih banyak spesies menjadi sensitif terhadap obat dan kapasitas untuk perlindungan silang menurun, tetapi juga muncul interaksi negatif, yang semakin meningkatkan sensitivitas anggota komunitas. Kami tertarik untuk memahami sifat mekanisme sensitisasi silang ini di masa mendatang.”
Sama seperti bakteri yang mereka pelajari, para peneliti juga mengambil strategi komunitas untuk studi ini, dengan menggabungkan kekuatan ilmiah mereka. Typas Group adalah pakar dalam pendekatan mikrobioma dan mikrobiologi eksperimental berthroughput tinggi, sementara Bork Group berkontribusi dengan keahlian mereka dalam bioinformatika, Zimmermann Group melakukan studi metabolomik, dan Savitski Group melakukan eksperimen proteomik. Di antara kolaborator eksternal, kelompok alumni EMBL Kiran Patil di Medical Research Council Toxicology Unit, University of Cambridge, Inggris Raya, memberikan keahlian dalam interaksi bakteri usus dan ekologi mikroba.
Sebagai percobaan berwawasan ke depan, penulis juga menggunakan pengetahuan baru tentang interaksi perlindungan silang ini untuk menyusun komunitas sintetis yang dapat menjaga komposisinya tetap utuh setelah perawatan obat.
“Studi ini merupakan batu loncatan untuk memahami bagaimana obat-obatan memengaruhi mikrobioma usus kita. Di masa mendatang, kita mungkin dapat menggunakan pengetahuan ini untuk menyesuaikan resep guna mengurangi efek samping obat,” kata Peer Bork, Ketua Kelompok dan Direktur di EMBL Heidelberg. “Untuk mencapai tujuan ini, kami juga mempelajari bagaimana interaksi antarspesies dibentuk oleh nutrisi sehingga kami dapat menciptakan model yang lebih baik untuk memahami interaksi antara bakteri, obat-obatan, dan inang manusia,” tambah Patil.